
400 850 6500

2020-01-13 1881浏览
A-level考试中,在选择学习课程的时候,数理化一直是大家选择的焦点,而化学的备考历来也是大家关注的重点,那么该如何备考A-level化学课程呢?很多同学都有这样的疑问,本文小编就为大家介绍一下A-level化学考试化学反应速率的特点和计算,希望能够对大家有所帮助。

一、化学反应速率的特点
通常用单位时间内反应物浓度的减少量或生成物浓度的增加量来表示化学反应速率。浓度常以mol/L为单位,时间常以min(分)或s(秒)为单位,化学反应速率的相应单位为mol/(L·min)或mol/(L·s)。
(1)化学反应速率是平均速率,均取正值。
(2)同一反应选用不同物质的浓度的改变量表示速率,数值可能不同,但表示的意义相同。
(3)在一定温度下,固体和纯液体物质单位体积里的物质的量保持不变,即物质的量浓度为常数,因此,它们的化学反应速率也被视为常数。因此,通常情况下不用化学反应体系中的固体和纯液体来表示化学反应速率。
二、化学反应速率的计算
(1)在解题过程中经常用到“起始量、转化量、某时刻量”的格式来分析、解决问题。如对于反应:mA + nB === pC + qD。A的起始浓度为a mol·L-1,B的起始浓度为b mol·L-1,反应进行到t1 s时,A消耗了x mol·L-1,则反应速率可计算如下:
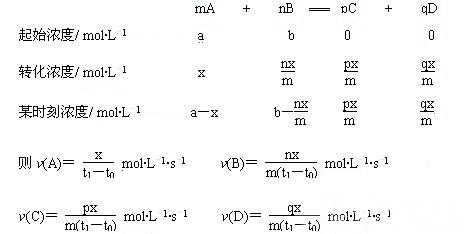
(2)对上述反应来说,在同一段时间内,v(A)、v(B)、v(C)、v(D)的数值不一定相同,但其表达的意义完全相同,都表示的是同一个反应在同一段时间内,反应向同一个方向进行的快慢。
(3)在同一段时间内,同一个反应中用不同的物质表示的反应速率之比等于相应物质的化学计量数之比即:v(A) : v(B) : v(C) : v(D) = m : n : p : q。
以上就是本文关于A-level化学考试化学反应速率的特点和计算的内容介绍了,希望能够对大家的复习有所帮助,如果还想了解更多关于alevel法律、alevel非全日制培训等方面的内容,可以咨询我们的客服哦~

上一篇 : O-level生物组成生物体的化合物介绍
下一篇 : 备考A-level生物课程易错知识点汇总
A/OLevel
![]() 苏公网安备32011302322644号增值电信业务经营许可证:苏B2-20190120 苏ICP备17009794号-16 Powered by marler.cn
苏公网安备32011302322644号增值电信业务经营许可证:苏B2-20190120 苏ICP备17009794号-16 Powered by marler.cn
2017-2021 AOLEVEL.COM.CN All Right Reserved.南京课窝教育科技有限公司版权所有